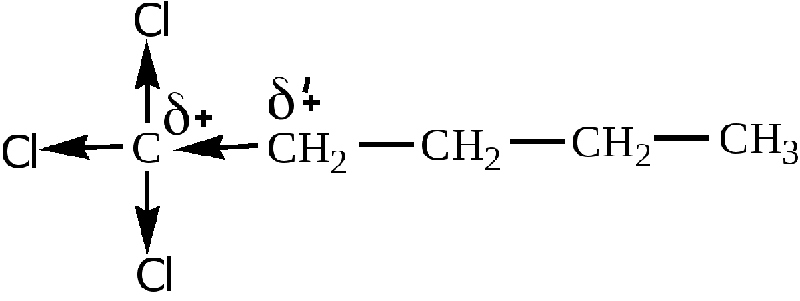Видео метод электронного баланса
Метод электронного баланса
Окислительно-восстановительные реакции. Электронный баланс. Подробнее

89. Как расставить коэффициенты реакции методом электронного баланса (закрепление) Подробнее

67. Метод электронного баланса Подробнее

Учимся составлять электронный баланс/овр/8класс Подробнее

Окислительно-восстановительные реакции. Метод электронного баланса. ЕГЭ Подробнее

Окислительно-восстановительные реакции. Метод электронно-ионного баланса. Подробнее

Составление ОВР методом электронного баланса Подробнее

Окислительно-восстановительные реакции в кислой среде. Упрощенный подход. Подробнее

Частая ошибка. Электронный баланс | ЕГЭ Химия | Лия Менделеева Подробнее

140. Расставляем коэффициенты методом электронного баланса Подробнее

Окислительно-восстановительные реакции. Видеоурок по химии 9 класс Подробнее

Тест В3. Расстановка коэффициентов методом электронного баланса Подробнее

ОГЭ ХИМИЯ 2019 Задание 20 ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ ОВР БАЛАНС Видеоурок ЕГЭ 8 класс Подробнее

Окислительно-восстановительные реакции. Электронный баланс Подробнее

«Электронный баланс VS Метод полуреакций» | ЕГЭ ХИМИЯ 2020 | Онлайн-школа СОТКА Подробнее

Химия. ОГЭ 2020 № 20 ОВР. Метод электронного баланса Подробнее

Окислительно-восстановительные реакции (ОВР). Что надо знать и как их решать Подробнее

ОГЭ химия. Решение окислительно-восстановительных реакций методом электронного баланса. Подробнее

Окислительно-восстановительные реакции в кислой среде. Продвинутый подход. Подробнее

Окислительно восстановительные реакции | Химия 8 класс #52 | Инфоурок Подробнее
Метод электронного баланса
Составляя любое уравнение химической реакции, следует соблюдать закон сохранения масс веществ — кол-во атомов в исходных веществах (левая часть уравнения) и в продуктах реакции (правая часть уравнения) должны совпадать.
Составляя уравнения окислительно-восстановительных реакций, следует также следить за суммой зарядов, которые у исходных веществ и в продуктах реакции должны быть равны.
В уравнениях ОВР в левой части обычно указывают первым вещество-восстановитель (отдает электроны), а затем — вещество-окислитель (принимает электроны); в правой части уравнения первым указывают продукт окисления, затем восстановления, а потом другие вещества, если они имеются.
Главное требование, которое необходимо соблюдать при составлении уравнений окислительно-восстановительных реакций, — кол-во электронов, которое отдал восстановитель, должно быть равно кол-ву электронов, принятых окислителем.
В основе метода электронного баланса лежит сравнение степеней окисления в исходных веществах и продуктах реакции, что подразумевает тот факт, что, составляющий уравнение ОВР методом электронного баланса, должен знать, какие вещества образуются в ходе реакции.
Примеры составления уравнений ОВР методом электронного баланса
1. Составить уравнение реакции алюминия с углеродом.
- Al+C → Al4C3
- В первую очередь, определяются элементы, меняющие свои степени окисления:
Al 0 +C 0 → Al4 +3 C3 -4 - Атом алюминия в ходе реакции отдает 3 электрона, меняя свою степень окисления с 0 на +3
Al 0 → Al +3
1Al 0 -3e — → 1Al +3 - Атом углерода принимает 4 электрона, меняя свою степень окисления с 0 на -4
C 0 → C +4
1C 0 +4e — → 1C -4 - Поскольку, число отданных и принятых электронов между атомами должно совпадать, следует сбалансировать уравнение, подобрав множители, для этого кол-во отданных алюминием электронов, записывают в схему реакции углерода, а кол-во электронов, принятых углеродом — в схему реакции алюминия:
- В итоге, алюминий отдает 4·3=12 электронов;
- углерод принимает 3·4=12 электронов
- Осталось определить стехиометрические коэффициенты, которые необходимо проставить перед формулами веществ, чтобы уравнять кол-во их атомов в левой и правой части уравнения;
- Кол-во атомов алюминия, вступающих в реакцию:
4·1Al 0 =4Al 0 - Кол-во атомов углерода, вступающих в реакцию:
3·1C 0 =3C 0 - Окончательный вид уравнения:
4Al 0 +3C 0 = Al4 +3 C3 -4
2. Составить уравнение реакции азотной кислоты с йодом.
- Схема реакции:
HNO3+I2 → HIO3+NO+H2O - Определяем элементы, меняющие свои степени окисления:
HN +5 O3+I2 0 → HI +5 O3+N +2 O+H2O - Азот меняет степень окисления с +5 на +2 — принимает 3 электрона, и является окислителем:
N +5 → N +2
N +5 +3e — → N +2 - Йод меняет степень окисления с 0 на +5 — отдает 5 электронов, и является восстановителем, но, поскольку молекула йода двухатомна, то в схеме она записывается в молекулярном виде, а кол-во отдаваемых электронов соответственно удваивается:
I2 0 → 2I +5
I2 0 -10e — → 2I +5 - Уравниваем заряды:
- Было до реакции 10·1N +5 =10N +5 , после реакции образовалось: 10·1N +2 =10N +2
- В реакцию вступило всего 6 атомов йода (3·2) или три молекулы 3I2, после реакции образовалось 3·2I +5 =6I +5 ;
- Расставляем найденные коэффициенты:
10HNO3+3I2 = 6HIO3+10NO+2H2O
3. Составить уравнение реакции соляной кислоты (концентрированной) с оксидом марганца (IV).
- HCl+MnO2 → Cl2+MnCl2+H2O
- HCl -1 +Mn +4 O2 → Cl2 0 +Mn +2 Cl2+H2O
- Соляная кислота является восстановителем, оксид марганца — окислителем.
- Атом хлора отдает свой электрон, но в правой части нулевой заряд имеет молекула хлора, состоящая из двух атомов, поэтому, для ее получения нужны 2 электрона от двух атомов хлора:
Cl -1 → Cl2 0
2Cl — -2e — → Cl2 0 - Атом марганца получает 2 электрона, снижая свою степень окисления с +4 до +2:
Mn +4 → Mn +2
Mn +4 +2e — → Mn +2 - Поскольку, хлор отдает два электрона, а марганец эти же два электрона принимает, оба коэффициента будут равны 2, и их можно сократить:
- Получаем уравнение, отличающееся от исходного только стехиометрическим коэффициентом 2, который стоит перед формулой соляной кислоты (два атома хлора отдают по одному электрону):
2HCl+MnO2 → Cl2+MnCl2+H2O - Осталось найти стехиометрические коэффициенты для остальных веществ, чтобы уравнять левую и правую части уравнения.
- В левой части уравнения 2 атома хлора, в правой — 4, чтобы уравнять атомы хлора, перед формулой соляной кислоты ставим 4, но, теперь в правой части уравнения получается на 2 атома водорода меньше, чтобы уравнять атомы водорода, перед молекулой воды ставим коэффициент 2 — теперь кол-во всех атомов в левой части и в правой части уравнения одинаково:
4HCl+MnO2 → Cl2+MnCl2+2H2O - Ионное уравнение реакции:
4H + +4Cl — +MnO2 = Cl2+Mn 2+ +2Cl — +2H2O
4. Составить уравнение реакции сероводорода с раствором калия перманганата в кислой среде.
- Схема реакции:
H2S+KMnO4+H2SO4 → S+MnSO4+K2SO4+H2O - Определяем элементы, меняющие свои степени окисления:
H2S -2 +KMn +7 O4+H2SO4 → S 0 +Mn +2 SO4+K2SO4+H2O - Сера меняет свою степень окисления с -2 до 0, т.е., отдает 2 электрона (сероводород — восстановитель):
S -2 → S 0
S -2 -2e — → S 0 - Марганец меняет свою степень окисления с +7 до +2, т.е., принимает 5 электронов (калия перманганат — окислитель):
Mn +7 → Mn +2
Mn +7 +5e — → Mn +2 - Электронные уравнения:
- 5H2S+2KMnO4+H2SO4 = S+MnSO4+K2SO4+H2O
- 5H2S+2KMnO4+3H2SO4 = 5S+2MnSO4+K2SO4+8H2O
- Ионное уравнение:
5H2S+2MnO4 — +6H + = 5S+2Mn 2+ +8H2O
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:

Код кнопки: 
Политика конфиденциальности Об авторе
Метод электронного баланса и ионно-электронный метод (метод полуреакций)
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение. Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
Метод электронного баланса
В его основе лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
- Сначала необходимо составить схему реакции: записать вещества в начале и конце реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
- Далее определим какие из соединений являются окислителем и восстановителем; найдем их степень окисления в начале и конце реакции:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6, таким образом, S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
- Составим электронные уравнения и найдем коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 ¦ 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 ¦ 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
- Далее надо уравнять количества атомов элементов, не изменяющих степень окисления, в такой последовательности: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
- Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления. При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде). В ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы: H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
- Сначала необходимо составить схему реакции: записать вещества в начале и конце реакции:
- Запишем уравнение в ионном виде, сократив те ионы, которые не принимают участие в процессе окисления-восстановления:
- Далее определим окислитель и восстановитель и составим полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + , образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
- Находим коэффициент для окислителя и восстановителя, учитывая, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O ¦2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + ¦5 восстановитель, процесс окисления
- Затем необходимо просуммировать обе полуреакции, предварительно умножая на найденные коэффициенты, получаем:
Сократив подобные члены, находим ионное уравнение:
- Запишем молекулярное уравнение, которое имеет следующий вид:
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — ¦2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O ¦3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
И еще один пример — составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 ¦2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O ¦1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Метод электронного баланса — правила и алгоритмы уравнивания реакций
Общие понятия
Взаимодействие исходных веществ с образованием новых, при котором ядра атомов остаются неизменными, называют химическими реакциями. Для них характерно перераспределение электронов. Исходные вещества называют реагентами, а прореагирующие — продуктами реакции. Превращение может происходить как сложных, так и простых элементов. Описываются они химическими уравнениями, состоящими из двух частей. Стрелка, разделяющая их, указывает направление протекания реакции.
Числа, стоящие перед веществами, участвующими в превращении, называют коэффициентами. Они указывают на количественную часть веществ. Любая реакция может происходить как с поглощением энергии, так и её выделением. В первом случае химическое уравнение называют эндотермическим, а во втором — экзотермическим.
Окислительно-восстановительными реакциями (ОВР) называют встречно-параллельные превращения с изменением степени окисления. Протекают они методом перераспределения электронов между акцептором — атомом окислителем и донором — восстановителем. Для составления уравнений, описывающих такого типа процесс, используют метод электронного баланса.
Примеры заданий предполагают, что в любой реакции, которую можно описать способом баланса, участвуют две сопряжённые окислительно-восстановительные пары. В итоге фактически возникают две полуреакции. Одна характеризуется увеличением электронов, а другая их отдачей. Таким образом, процессы окисления и восстановления не могут протекать друг без друга и не изменять степень окисления элементов.
Ионы или атомы, забирающие электроны называют окислителями, а отдающие — их восстановителями. Сложность записи таких уравнений заключается в правильном подборе количества молей возникающих соединений. Уравнивающие коэффициенты могут принимать только целые значения. Конкурентом метода баланса в химии является способ полуреакций. Первый отличается простотой и используется в том случае, когда реакция происходит в газообразной среде. Второй же более подходит для реакций, проходящих в жидкости.
Суть метода
Способ электронного баланса предназначен для облегчения решения заданий по уравниванию двух частей уравнения. В его сути лежит возможность расстановки коэффициентов для окислительно-восстановительной реакции с использованием степени окисления. Впервые с объяснением способа знакомят в восьмом классе на уроке неорганической химии.
В школьных учебниках часто приводится следующая последовательность действий для установления балансировки в ОВР:

- В уравнении определяют сложные и простые степени окисления.
- Реакцию переписывают с расстановкой степени окисления. При этом вещества, в которых изменяется степень во всех связях, выделяют любым способом, например, подчёркиванием.
- Находят окислитель, восстановитель, и в случае присутствия, нейтральный элемент.
- Составляют уравнение баланса с выделением внутренних коэффициентов.
- Определяют наименьшее общее кратное.
- Подставляют вычисленные коэффициенты в уравнение.
Классический способ, с помощью которого можно уравнять химические выражения, основан на законе сохранения массы, когда методом подбора находятся коэффициенты до начала реакции и после её окончания. Но для ОВР их подобрать очень сложно или невозможно. Поэтому и используют способ электронного баланса, который подходит как для простых, так и сложных реакций.
Степени окисления
Определение коэффициентов методом баланса непосредственно связано с расстановкой валентности. Не зная, как правильно выполнить эту операцию, уравнять ОВР будет невозможно. Под окислением элемента понимается значение заряда его атома. Этот ион может быть условным или реальным.
Существует несколько видов химических связей. Одними из них могут быть ковалентная и ионная. И в том, и другом случае между атомами образовывается пара. В первом случае пара смещается в сторону отрицательно заряженного атома, а во втором полностью переходит к более электроотрицательной частице. Поэтому под реальным зарядом понимается процесс, характеризующийся ионной связью, а условным — возникновение заряда при ковалентной.
Например, ионное соединение NaCl = Na 1+ + Cl 1- . Атом натрия имеет один электрон, который в ионном соединении полностью переходит к более отрицательному атому. То есть, электрон натрия отдаётся полностью атому хлора. При этом атом, утратив один ион, приобретает заряд равный один плюс. Хлор же, получая дополнительный электрон, меняет заряд на один минус.
В химии принято заряды обозначать сначала цифрой, а после ставить знак, а степень окисления наоборот. Поэтому правильной записью с указанием валентности для рассматриваемого примера будет выражение вида: Na +1 Cl -1 .
Для ковалентной полярной связи, например, молекулы HCl, общая электронная пара лишь смещается в сторону хлора. На атомах возникают частичные дельта-плюс и минус заряды. Но при расстановке значений на это внимания не обращают. Атом водорода полностью отдаёт свой электрон атому хлора. Соответственно, степень будет выглядеть как H +1 Cl -1 .
Следует помнить, что существуют элементы, которые всегда имеют постоянную валентность:

- Первую — щелочные металлы и фтор.
- Вторую — металлы II группы, главной подгруппы и кислород.
- Третью — алюминий.
Остальные же вещества характеризуются переменной валентностью. При описании реакции характерно выделение и гидроксильной группы. Для соединения ОН значение ионов указывается единым. Например, Na +1 (OH) -1 . Проверку правильности расстановки зарядов можно выполнить по правилу электронейтральности, согласно которому сумма положительных электронов должна быть равна сумме отрицательных.
Простой расчёт
Разобраться в сути способа поможет простой пример. Пусть необходимо расставить коэффициенты в реакции соединения оксида меди с азотной кислотой. Первым делом необходимо записать схему сложения: CuO + NH3 = Cu + N2 +H2O. Теперь нужно расставить валентность для каждого элемента. Делать это следует внимательно, ведь от того, насколько верно будет указана валентность, зависит правильность дальнейших действий.
Опираясь на таблицу Менделеева можно утверждать, что правильная степень окисления будет выглядеть для рассматриваемого выражения следующим образом: Cu +2 O -2 + N -3 H +1 3 = Cu 0 + N 0 2 +H +1 2O -2 . Теперь нужно отметить те элементы, которые поменяли свою валентность. Это медь, была +2, а стала 0, и азот, изменивший своё значение с -3 до 0.
На третьем шаге выписывают схемы уравнений полуреакций, изменивших окисление:
- Cu +2 — Cu 0 . Эта запись говорит, что два электрона были приняты медью и она стала нулевой. Обозначают этот процесс записью вида +2 e.
- 2N -3 — N 0 2. Тут следует обратить внимание на то, что при составлении полуреакций для молекул простых веществ обязательно следует указывать индексы. В рассматриваемом случае это двойка. Соответственно, такие выражения следует тоже уравнять. Поэтому в левой части ставится коэффициент два. Анализируя полуреакцию, можно прийти к выводу, что было -6 атомов, а стало ноль. То есть азот отдал шесть электронов. Записывается это как -6 e.
Закон сохранения заряда говорит о том, что электроны не могут взяться ниоткуда и пропасть никуда. Иными словами, какое их количество отдал восстановитель, то же их число должно быть принято окислителем.
В рассматриваемом примере получается, что два электрона были приняты, а шесть отданы. Так не бывает, поэтому нужно найти, где же потерялась разница. Для полученных чисел ищется наименьший общий знаменатель. Без остатка на них делится шесть. Выполнив действие, получают два опорных коэффициента: три и один. Таким образом, перед медью нужно поставить тройку, а азотом единицу: 3Cu +2 O -2 + 2N -3 H +1 3 = 3Cu 0 + N 0 2 +H +1 2O -2 .
Опираясь на полученные значения, проводят стандартную процедуру уравнивания: 3Cu +2 O -2 +2N -3 H +1 3 = 3Cu 0 + N 0 2 + 3H +1 2O -2 . Задача считается выполненной. Пожалуй, ещё можно указать, что медь в уравнении является окислителем, а азот — восстановителем.
Пример сложного соединения
Научившись решать простые задания можно переходить к формулам и сложнее. Например, соединению бромида и перманганата калия с серной кислотой. Схема реакции будет выглядеть следующим образом: KBr + KMnO4 + H2SO4 → MnSO4 + Br2 + K2SO4 + H2O.
Согласно правилу, нужно расставить ионны для каждого элемента: K +1Br+1 + K +1 Mn +7 O -2 4 + H +1 2S +6 O -2 4 → Mn +2 S +6 O -2 4 + Br02 + K +1 2 S +6 O -2 4 + H +1 2O -2 . В уравнении только два элемента изменили степень. Это марганец, который был +7, а стал +2, и бром, поменявший свою валентность с -1 до нуля.

Составляя уравнения полуреакций, проводят анализ. Марганец до реакции был + 7, то есть до нулевого значения ему не хватало семь единиц. После реакции же он стал +2, а значит, до нуля стало не хватать два электрона. Исходя из этого, можно утверждать, что марганец принял пять электронов: +5e.
Вторая полуреакция состоит из брома. Был он в степени -1, а стал в нулевой. При этом индекс у него стал два. Значит, первоначально в реакцию должны были вступить два атома брома. Следовательно, в исходном состоянии было 2*(-1) = -2 электрона, а после стало ноль. То есть бром отдал два электрона: — 2e.
Интересной особенностью метода является закономерность, что при составлении полуреакций в обязательном порядке в одной из них будут отдаваться электроны, а в другой забираться. Полученные уравнения будут иметь следующий вид:
Mn +7 — Mn +2 |+5e |5.
2Br -1 — Br 0 2 |-2e |2.
Для продолжения решения полученные цифры нужно привести к общему знаменателю. В качестве уравнителя здесь будет число десять. Разделив на него количество электронов, находят два опорных коэффициента. Для марганца это будет двойка, а брома — пятёрка.
Полученные числа подставляют в уравнение:
2KBr + 10KMnO4 + H2SO4 → 5 Br2 + 2MnSO4+ K2SO4 + H2O.
Перед бромом должна стоять пятёрка, а вот перед бромом два следует поставить уже десятку. Проверяем, в левой части десять ионов брома вступило в реакцию и десять получилось в прореагирующей части. Возле марганца ставим двойку, соответственно, изменяется и количество калия. В левой части получается 12 атомов, а в правой только два. Поэтому справа возле калия нужно поставить шесть. Аналогично уравнивают серу, водород и кислород.
В итоге полным правильным уравнением будет следующая химическая формула: 2KBr + 10KMnO4 + 8H2SO4 → 5 Br2 + 2MnSO4+ 6K2SO4 + 8H2O. Полученное выражение дальше править уже не нужно. Глядя на него можно утверждать, что марганец является окислителем, а бром восстановителем.
Использование онлайн-калькулятора

В интернете существуют сервисы, использование которых позволяет не только быстро выполнить уравнивание химических уравнений, но и получить нужные знания для самостоятельных вычислений. Называются они химическими онлайн-калькуляторами. Метод электронного баланса сам по себе несложен, но порой составление полуреакций может занять длительное время. Поэтому даже опытные пользователи прибегают к их помощи.
Эти порталы привлекательны тем, что решить поставленную задачу на них сможет даже тот, кто совершенно не разбирается в химии. Доступны онлайн-калькуляторы любому, кто имеет доступ к интернету.
От пользователя требуется загрузить сайт, ввести в предоставленную форму уравнение и кликнуть по меню «Рассчитать». Через две — три секунды система выдаст правильный ответ. При этом услуга предоставляется бесплатно и без ограничений.